INTRODUCCIÓN
OBJETIVOS
- Reconocer la clasificación de Hidrocarburos Aromáticos.
- Distinguir los diferentes nombres de Aromáticos.
- Identificar la utilidad de los Hidrocarburos Aromáticos.
- Analizar los nombres de los Hidrocarburos Aromáticos.
MARCO TEÓRICO
BENCENO
Es un producto físico conocido y de extenso uso industrial, se obtiene como subproducto bolatin de la fabricación del choque de la hulla (carbón) es el mas simple de una clase de sustancias llamados hidrocarburos aromáticos.

El benceno se caracteriza por una inusual estabilidad, que le viene dada por la particular disposición de los dobles enlaces conjugados. Formas resonantes. Aunque su estructura sea la de un alqueno poliinsaturado (ciclohexa-1,3,5-trieno), es decir tiene más de un doble enlace entre sus carbonos, presenta formas resonantes las cuales le confieren una gran estabilidad; de forma molecular C6H6, con forma de anillo.
CARACTERÍSTICAS
- Es incoloro, de aroma dulce y sabor ligeramente amargo, similar al de la hiel. Se evapora al aire rápidamente y es poco soluble en agua. Es sumamente inflamable, volátil y se forma tanto en procesos naturales como en actividades humanas.

- La representación de los tres dobles enlaces se debe a Friedrich Kekulé, quien además fue el descubridor de la estructura anular de dicho compuesto y el primero que lo representó de esta manera.

- Los dobles enlaces al estar alternados le otorgan a la molécula de benceno sus características tan especiales. Cada carbono presenta en el benceno hibridación Sp2. Estos híbridos se usarán tanto para formar los enlaces entre carbono como los enlaces entre los carbonos y los hidrógenos.
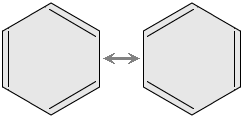
- Espectroscópicamente, se ha determinado que:
- Todos los enlaces C-C tienen la misma longitud (1,39 Armstrong) que es intermedia entre un enlace simple (1,54 Armstrong) y uno doble (1,34 Armstrong ).
- Todos los ángulos de enlace C-C-C son de 120°ambos casos se forma el mismo producto, el ciclohexano.
- Se puede obtener una medida cuantitativa de la estabilidad, determinando la cantidad de calor liberado cuando se hidrogenan el benceno y el ciclohexeno.
- Si los tres dobles enlaces del benceno fueran equivalentes a tres dobles enlaces etilénicos (-C=C-), el calor liberado por hidrogenación completa en presencia de un catalizador, sería tres veces mayor que el liberado por hidrogenación del ciclohexeno.
- Todos los carbonos están hibridizados Sp2, luego la estructura básica del benceno considera un anillo plano de 6 átomos de carbono, en cada uno de ellos hay un orbital p. Como la distancia C-C es la misma y pequeña (1,39 Armstrong ), los orbitales p pueden superponerse efectivamente formando una nube electrónica homogénea.

- Generalmente los compuestos mas sencillos tienen nombres comunes aunque no guardan ralacion con su estructura, sirve como base para nombrar sus derivados.
- La IUPAC a propuesto una nomenclatura sistemática en la cual los compuestos se pueden nombrar como alquin o alquininbenceno.
AROMÁTICOS
En los inicios de la química orgánica, la palabra aromático se usaba para describir sustancias fragantes como el benzaldehído (de cerezas, durazno y almendras), el tolueno (del bálsamo de tolú) y el benceno (del destilado del carbono); por lo que se asocio la aromaticidad con los compuestos que contenían el anillo benceno. Sin embargo, pronto se comprendió que las sustancias agrupadas como aromáticas se comportaban de manera químicamente distinta de cómo lo hacen la mayoría de los otros compuestos orgánicos, por lo que la teoría moderna ha extendido el concepto de aromaticidad para incluir a sistemas policíclicos como el naftaleno, antraceno, fenantreno e incluso a ciertos cationes y aniones que poseen el número adecuado de electrones pi y que son capaces de crear formas resonantes.
Las especies aromáticas cumplen tres condiciones:
- Sus moléculas son cíclicas.
- Sus moléculas son planas.
- Sus moléculas tienen electrones compartidos en número igual a 4n+2 (regla de hückell)
- Su estructura debe ser cíclica y debe contener enlaces dobles conjugados.
- Cada átomo de carbono del anillo debe presentar hibridación Sp2, u ocasionalmente Sp, con al menos un orbital p no hibridizado.
- Los orbitales p deben solaparse para formar un anillo continuo de orbitales paralelos. La estructura debe ser plana o casi plana para que el solapamiento de los orbitales p sea efectivo.
PROPIEDADES FÍSICAS
- Poseen una gran estabilidad debido a las múltiples formas resonantes que presenta.
- Son insolubles en agua
- Muy solubles en disolventes no polares como el éter.
- Es un líquido menos denso que el agua. Sus puntos de ebullición aumentan, conforme se incrementa su peso molecular.
- Los puntos de fusión no dependen únicamente del peso molecular sino también de la estructura.
PROPIEDADES QUÍMICAS
- Reacción de Halogenación: En presencia del hierro o su-sales férricas que actúan como catalizadores cloro y bromo reaccionan fácilmente con los aromáticos para formar el derivado halogenado de sustancia.

- Reacción de Nitración: La sustitución de un átomo de hidrógeno unido al núcleo aromático benceno por el grupo nitro se consigue con el uso del ácido nítrico. el producto de la sustitución se denomina nitro-benceno y la reacción nitración.

- Reacción de Friedel Crafts o Aquilación: Los haluros de alquilo,en presencia de cloruro de aluminio reacciona con el benceno para formar compuestos de sustitución alquilicas en los cuales un grupo alquilico sustituye a un átomo de hidrógeno en el anillo.
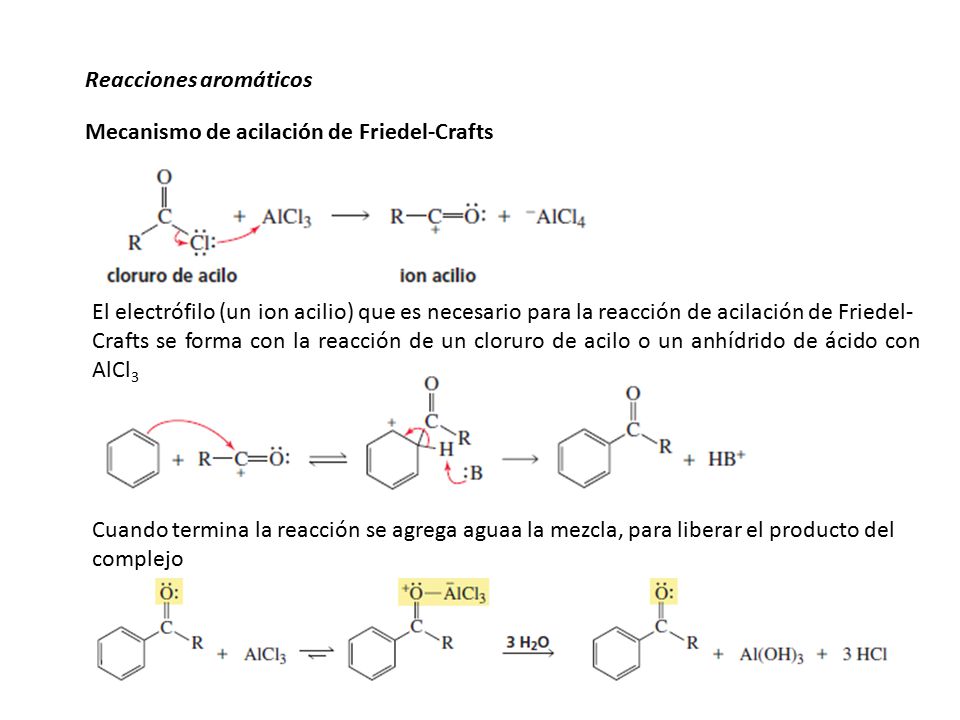
NOMENCLATURA
- Derivados mono-sustituidos: Se nombra primero el radical (prefijo del nombre sustituyente) y se termina en la palabra benceno. Como los 6 átomos del carbono en el benceno son equivalentes, solo existe un derivado mono sustituido. la sustitución de cualquiera de los H en el anillo determina el mismo compuesto.
Ejemplos:


- Derivados Destituidos: Se originan 3tipos de is-omeros de posición que se designan con los prefijos:
- Orto: 1-2

Nombre: O-dimetilbenceno
- Meta: 1-3 (m)
Nombre: m-dimetilbenceno
- Para: 1-4 (p)

Nombre: p-dimetilbenceno
- Compuestos con nombres propios:
Ejemplos:

Nombre: Anilina

Nombre: Fenol

Nombre: Tolueno

Nombre: Ácido Benzoico

Nombre: Nitrobenceno

Nombre: Benzaldehido

Nombre: Estireno

Nombre: Para- xileno

Nombre: Ácido Gálico
- Si el largo de la cadena es mayor a 6 carbonos

Nombre: 3-FENIL NONANO

Nombre: (n)- PROPIL BENCENO
- Compuestos orgánicos Polisustituidos: Con este nombre se conocen los derivados aromáticos en los cual se han remplazado 3 o más hidrógenos por otros grupo o átomos.
En estos casos es necesario numerar el anillo bajo las siguientes reglas:
- El número 1 corresponde al radical con menor orden alfabético.
- La numeración debe continuarse hacia donde este el radical más cercano para obtener la serie de números más pequeña posible. Si hay dos radicales a la misma distancia, se selecciona el de menor orden alfabético; si son iguales se toma el siguiente radical más cercano
- Todos los átomos de carbono deben numerarse, no solo los que tengan sustituyente.
- Al escribir el nombre se ponen los radicales en orden alfabético terminando con la palabra benceno.
Ejemplos:

Nombre: 1-bromo-3-etil-4-metilbenceno
El número 1 corresponde al bromo que es el radical de menor orden alfabético. Se numera hacia la derecha porque en ese sentido quedan los números más pequeños posibles.
- Cuando tiene más de 2 sustituyentes: Se nombran por orden alfabético dándole la menor numeración a los sustituyentes presentes, o en base a un compuesto aromático de nombre trivial.

Nombre: 2-bromo-1-metil-4-nitrobenceno

Nombre: 2, 4,6-tribromofenol
- Hidrocarburos Condensados: son moléculas con átomos de carbono comunes a 2 o mas anillos bencenicos los mas importantes:

Nombre: Naflateno

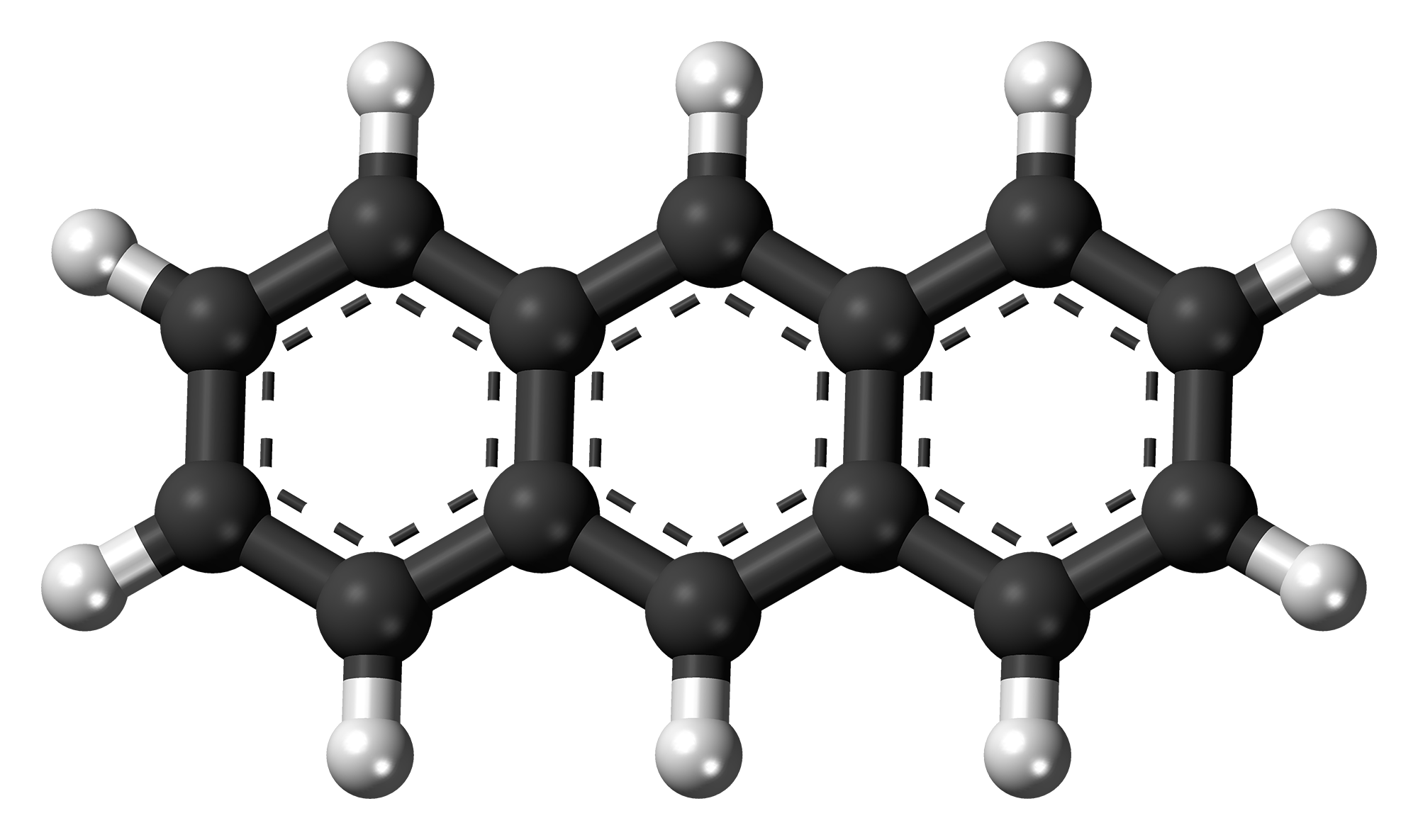
Nombre: Antraceno

Nombre: Fenantreno

Nombre:Fireno
APLICACIONES DE LOS AROMÁTICOS
- Tolueno: Se emplea en la fabricación de explosivos y colorantes.

- Clorobenceno: Este compuesto no tiene nombrecomún. Es un líquido incoloro de oloragradable empleado en la fabricacióndel fenol y del DDT.

- Fenol: Fue el primer desinfectante utilizado,pero por su toxicidad ha sidoreemplazado por otros menosperjudiciales.Se emplea para prepararmedicamentos, perfumes, fibras textilesartificiales, en la fabricación decolorantes. En aerosol, se utiliza paratratar irritaciones de la garganta. Enconcentraciones altas es venenoso.

- Anilina: Es la amina aromática más importante.Es materia prima para la elaboración decolorantes que se utilizan en la industriatextil. Es un compuesto tóxico.

- Antraceno: Se utiliza para proteger postes ydurmientes de ferrocarril de agentesclimatológicos y del ataque de insectos.
- Ácido Benzoico: Se utiliza como desinfectante y como conservador de alimentos
EJERCICIOS
CORRECCIÓN
EJERCICIOS 2
EJERCICIOS 3
EJERCICIO 4
WEBGRAFÍA
- http://aro-maticos.blogspot.com/2011/06/estructura-y-nomenclatura.html
- http://hidrocarburos-tess.blogspot.com/
- http://centros.edu.xunta.es/iesasardineira/web_CS/qo/nomenclatura/nomenorgan/hidrocarburos/aromaticos.php
- http://dianacarolinahernandes.blogspot.com/
- http://www.100ciaquimica.net/fororg/ejer.htm
- https://www.liceoagb.es/quimiorg/hpotatoes/arom2.htm
- https://es.educaplay.com/recursos-educativos/1974768-nomenclatura_de_los_aromaticos.html
- https://es.educaplay.com/recursos-educativos/1158432-hidrocarburos_aromaticos.html
